- Почетна
-
Седми разред
-
Осми разред
- Неметали, оксиди неметала, киселине >
- Метали, оксиди метала и хидроксиди (базе) >
- Соли >
- Електролитичка дисоцијација киселина, хи >
- Неметали, метали и соли (утврђивање)
- Увод у органску хемију >
- Угљоводоници >
- Органска једињења са кисеоником >
- Биолошки важна органска једињења >
- Хемија животне средине >
- Провери своје знање (средња школа)
- Периодни систем елемената
- Занимљивости из света хемије
- Моја хемија
Метали имају мали број валентних електрона. Да би постигли распоред електрона какав има њима најближи племенити гас, атоми метала теже да се ослободе валентних електрона. Атоми метала се понашају као да имају вишак електрона. Атомима неметала недостају електрони.
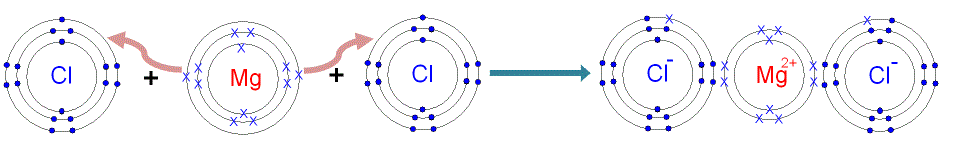
Када атоми метала граде хемијску везу са атомима неметала долази до примо - предаје електрона. Атоми метала предају своје електроне атомима неметала.
Када атоми метала граде хемијску везу са атомима неметала долази до примо - предаје електрона. Атоми метала предају своје електроне атомима неметала.
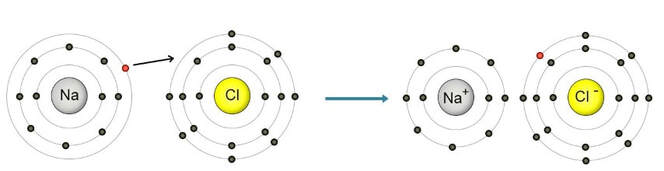
Јонска веза између атома метала и атома неметала формира се тако што атоми метала (натријума) предају своје валентне електроне атомима неметала (хлора). На тај начин у атому натријума, који је пре примопредаје електрона имао исти број протона и електрона, остаје више протона, па он постаје позитивно наелектрисана честица. Када прими један електрон, атом хлора који је такође имао исти број протона и електрона, има више електрона, па постаје негативно наелектрисан.
11Na K2 L8 M1
10Ne K2 L8
17Cl K2 L8 M7
18Ar K2 L8 M8
..
Na ∙ + ∙ Cl: → [Na+] [Cl-]
..
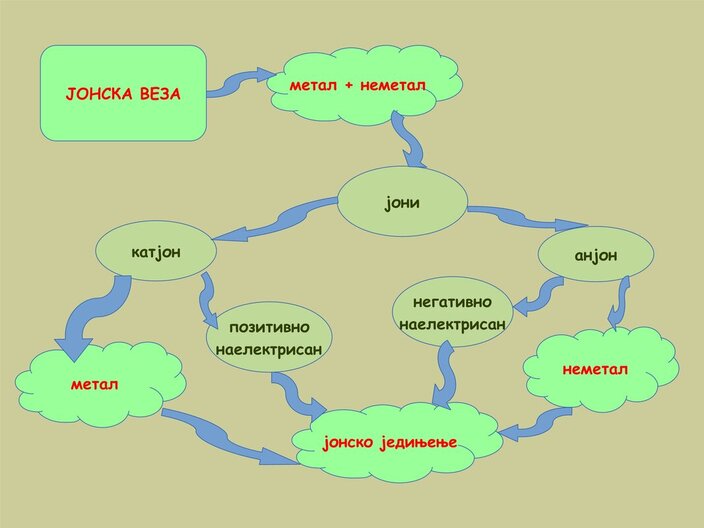
Наелектрисане честице се називају јони. Позитивно наелектрисани јони су катјони, а негативно наелектрисани јони су анјони. Између супротно наелектрисаних јона се јавља електростатичко привлачно дејство које се назива јонска веза. Натријум постиже стабилност неона (10 е-), а хлор стабилност аргона (18 е-).
Јони су правилно распоређени у простору и такав правилан распоред јона у простору назива се кристална решетка. Формула јонског једињења не представља молекул, већ однос јона у кристалној решетки.
11Na K2 L8 M1
10Ne K2 L8
17Cl K2 L8 M7
18Ar K2 L8 M8
..
Na ∙ + ∙ Cl: → [Na+] [Cl-]
..
Наелектрисане честице се називају јони. Позитивно наелектрисани јони су катјони, а негативно наелектрисани јони су анјони. Између супротно наелектрисаних јона се јавља електростатичко привлачно дејство које се назива јонска веза. Натријум постиже стабилност неона (10 е-), а хлор стабилност аргона (18 е-).
Јони су правилно распоређени у простору и такав правилан распоред јона у простору назива се кристална решетка. Формула јонског једињења не представља молекул, већ однос јона у кристалној решетки.
Питања и одговори:
1. Атоми којих елемената се повезују јонском везом?
- Метали и неметали.
2. Шта су јони?
- Наелектрисане честице.
3. Шта су катјони, а шта анјони?
- Позитивно наелектрисане честице – катјони, негативно наелектрисане – анјони.
4. Како се мења број електрона када настају катјони, а како када настају анјони?
- Када настају катјони број електрона се смањује, када настају анјони број електрона се повећава.
5. Како су распоређени јони у простору?
- Јони су правилно распоређени у простору и такав правилан распоред јона у простору назива се кристална решетка.
6. Шта представља формула јонског једињења?
- Формула јонског једињења не представља молекул, већ однос јона у кристалној решетки.
1. Атоми којих елемената се повезују јонском везом?
- Метали и неметали.
2. Шта су јони?
- Наелектрисане честице.
3. Шта су катјони, а шта анјони?
- Позитивно наелектрисане честице – катјони, негативно наелектрисане – анјони.
4. Како се мења број електрона када настају катјони, а како када настају анјони?
- Када настају катјони број електрона се смањује, када настају анјони број електрона се повећава.
5. Како су распоређени јони у простору?
- Јони су правилно распоређени у простору и такав правилан распоред јона у простору назива се кристална решетка.
6. Шта представља формула јонског једињења?
- Формула јонског једињења не представља молекул, већ однос јона у кристалној решетки.