- Почетна
-
Седми разред
-
Осми разред
- Неметали, оксиди неметала, киселине >
- Метали, оксиди метала и хидроксиди (базе) >
- Соли >
- Електролитичка дисоцијација киселина, хи >
- Неметали, метали и соли (утврђивање)
- Увод у органску хемију >
- Угљоводоници >
- Органска једињења са кисеоником >
- Биолошки важна органска једињења >
- Хемија животне средине >
- Провери своје знање (средња школа)
- Периодни систем елемената
- Занимљивости из света хемије
- Моја хемија
Сваки атом је одређен са два броја – атомски број који се означава са Z и масеним бројем А.
Атомски број представља број протона у језгру неког атома односно број електрона у електронском омотачу, јер је атом електронеутрална честица пошто садржи исти број протона у језгру и електрона у електронском омотачу.
Масени број представља збир протона и неутрона у језгру атома.
Z = N(p+) = N(e-)
A = N(p+) + N(nº), N(nº) = A – N(p+) = A - Z
Атомски број се пише у доњем левом углу испред симбола хемијског елемента.
Масени број се пише у горњем левом углу испред симбола хемијског елемента.
A
Z Е
Атоми различитих елемената разликују се по броју протона, а атоми истог елемента имају исти број протона у језгру.
Питања и одговори:
1. Шта је атомски број?
- Атомски број показује број протона у језгру неког атома, тј. број електрона у електронском омотачу.
2. Шта је масени број?
- Масени број представља збир протона и неутрона у језгру неког атома.
3. Где се пише атомски број?
- Атомски број се пише у доњем левом углу испред симбола елемента.
4. Где се пише масени број?
- Масени број се пише у горњем левом углу испред симбола елемента.
5. Одреди бој протона, електрона и неутрона у атомима следећих хемијских елемената:
– кисеоника, O Z=8, A=16, N(p+) = N(e-) = 8, N(nº) = 16 - 8 = 8
– азота, N Z=7, A=14, N(p+) = N(e-) = 7, N(nº) = 14 - 7 = 7
– натријума
– калијума
– алуминијума
– гвожђа
6. Шта су изотопи?
- То су атоми истог елемента који имају исти атомски, а различити масени број.
У природи могу постојати атоми истог елемента који се разликују по броју неутрона. Ти атоми се називају изотопи. Изотопи су дакле атоми истог хемијског елемента који имају исти број протона, различит број неутрона. Изотопи имају исти атомски, а различит масени број.
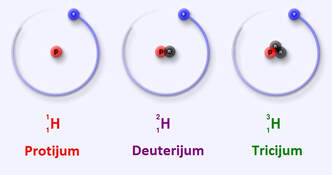
Најзначајни пример је водоник који се у природи среће у облику три изотопа – протијум, деутеријум и трицијум.
Обележавамо их на следећи начин:
Атомски број представља број протона у језгру неког атома односно број електрона у електронском омотачу, јер је атом електронеутрална честица пошто садржи исти број протона у језгру и електрона у електронском омотачу.
Масени број представља збир протона и неутрона у језгру атома.
Z = N(p+) = N(e-)
A = N(p+) + N(nº), N(nº) = A – N(p+) = A - Z
Атомски број се пише у доњем левом углу испред симбола хемијског елемента.
Масени број се пише у горњем левом углу испред симбола хемијског елемента.
A
Z Е
Атоми различитих елемената разликују се по броју протона, а атоми истог елемента имају исти број протона у језгру.
Питања и одговори:
1. Шта је атомски број?
- Атомски број показује број протона у језгру неког атома, тј. број електрона у електронском омотачу.
2. Шта је масени број?
- Масени број представља збир протона и неутрона у језгру неког атома.
3. Где се пише атомски број?
- Атомски број се пише у доњем левом углу испред симбола елемента.
4. Где се пише масени број?
- Масени број се пише у горњем левом углу испред симбола елемента.
5. Одреди бој протона, електрона и неутрона у атомима следећих хемијских елемената:
– кисеоника, O Z=8, A=16, N(p+) = N(e-) = 8, N(nº) = 16 - 8 = 8
– азота, N Z=7, A=14, N(p+) = N(e-) = 7, N(nº) = 14 - 7 = 7
– натријума
– калијума
– алуминијума
– гвожђа
6. Шта су изотопи?
- То су атоми истог елемента који имају исти атомски, а различити масени број.
У природи могу постојати атоми истог елемента који се разликују по броју неутрона. Ти атоми се називају изотопи. Изотопи су дакле атоми истог хемијског елемента који имају исти број протона, различит број неутрона. Изотопи имају исти атомски, а различит масени број.
Најзначајни пример је водоник који се у природи среће у облику три изотопа – протијум, деутеријум и трицијум.
Обележавамо их на следећи начин: