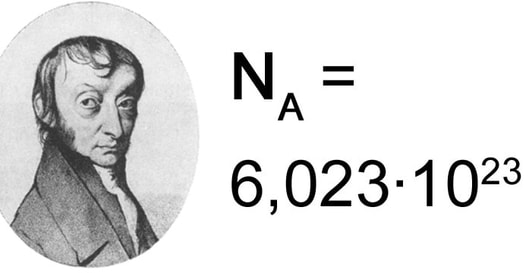- Почетна
-
Седми разред
-
Осми разред
- Неметали, оксиди неметала, киселине >
- Метали, оксиди метала и хидроксиди (базе) >
- Соли >
- Електролитичка дисоцијација киселина, хи >
- Неметали, метали и соли (утврђивање)
- Увод у органску хемију >
- Угљоводоници >
- Органска једињења са кисеоником >
- Биолошки важна органска једињења >
- Хемија животне средине >
- Провери своје знање (средња школа)
- Периодни систем елемената
- Занимљивости из света хемије
- Моја хемија
Физичка величина количина супстанце односи се на број честица супстанце.
Она нам говори колико има честица (атома, молекула, јона) неке супстанце.
Количина супстанце је једна од седам основних физичких величина.
Ознака за ову величину је n.
Јединица за количину супстанце је мол (mol).
Један мол супстанце јесте она количина супстанце која садржи 6,02 · 10²³ честица.
Овај број први је одредио научник Авогадро и по њему се назива Авогадров број, Na = 6,02 · 10²³
Она нам говори колико има честица (атома, молекула, јона) неке супстанце.
Количина супстанце је једна од седам основних физичких величина.
Ознака за ову величину је n.
Јединица за количину супстанце је мол (mol).
Један мол супстанце јесте она количина супстанце која садржи 6,02 · 10²³ честица.
Овај број први је одредио научник Авогадро и по њему се назива Авогадров број, Na = 6,02 · 10²³
Један мол различитих супстанци има исти број честица и углавном различиту масу.
Масу једног атома или молекула не можемо измерити, али масу једног мола супстанце можемо.
Моларна маса показује колико грама неке супстанце има у једном молу те супстанце.
Моларна маса (М) је однос масе супстанце (m) и њене количине (n).
M = m / n
Јединица за моларну масу је g/mol.
Моларна маса има исту бројну вредност као релативна атомска маса за атоме, односно релативна молекулска маса за молекуле или јонска једињења.
Натријум изграђују атоми. Релативна атомска маса натријума је 23, па је маса једног мола атома натријума 23 грама.
М = Аr · g/mol, за супстанце које изграђују атоми.
Воду чине молекули. Релативна молекулска маса воде је 18, (Mr (H2O)= 2· Ar (H) + Ar (O) = 2 · 1 + 16 = 18) па је маса једног мола молекула воде 18 грама.
М = Mr · g/mol, за супстанце које изграђују молекули или јони (супстанце које се представљају формулама).
1. Релативна молекулска маса угљен - диоксида, CO2 је 44. Колика је његова моларна маса?
Mr (CO2) = 44
M = Mr · g/mol
M (CO2) = 44 · g/mol
М (CO2) = 44 g/mol
2. Колика је моларна маса калцијум-оксида, CaO, ако знамо да 0,5 mol има масу од 28 g?
n= 0,5 mol; m = 28 g; M = ?
M = m / n
M = 28 g / 0,5 mol = 56 g / mol
Питања и задаци:
1. Колико износи Авогадров број?
2. Колико износи моларна маса азотне киселине ако знамо да је њена релативна молекулска маса 63?
3. Узорак кухињске соли масе 117 грама има 2 мола супстанце. Израчунајте моларну масу кухињске соли?