- Почетна
-
Седми разред
-
Осми разред
- Неметали, оксиди неметала, киселине >
- Метали, оксиди метала и хидроксиди (базе) >
- Соли >
- Електролитичка дисоцијација киселина, хи >
- Неметали, метали и соли (утврђивање)
- Увод у органску хемију >
- Угљоводоници >
- Органска једињења са кисеоником >
- Биолошки важна органска једињења >
- Хемија животне средине >
- Провери своје знање (средња школа)
- Периодни систем елемената
- Занимљивости из света хемије
- Моја хемија
Хемијске везе
Све у природи тежи што већој стабилности. Већина атома у природи није стабилна, сем атома племенитих гасова. Због тога се само племенити гасови у природи могу наћи у облику слободних атома. Атоми осталих хемијских елемената се удружују да би створили стабилне целине.
Атоми племенитих гасова се у природи могу наћи у слободном стању јер они у последњем енергетском нивоу поседују по осам електрона, изузев хелијума који има попуњен само један енергетски ниво у коме се налазе два електрона, што је и максималан број електрона за први енергетски ниво. Тако да кажемо да племенити гасови поседују стабилан октет односно стабилан дублет електрона.
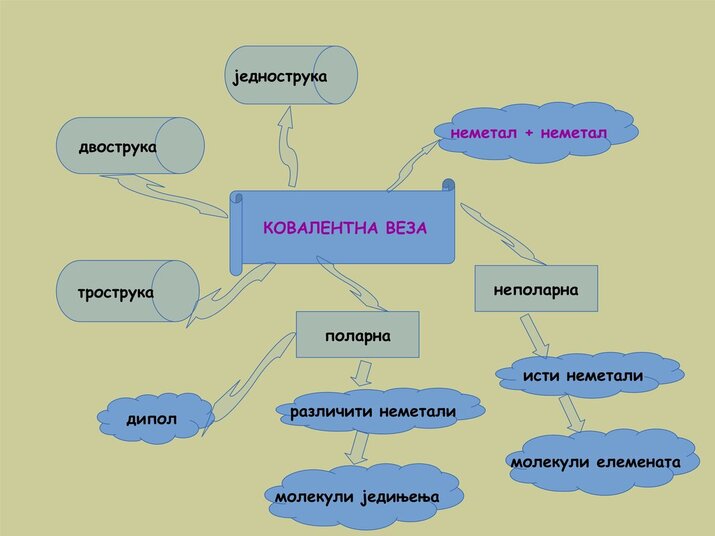
Овом броју електрона у последњем енергетском нивоу теже сви остали атоми у природи. Због ове тежње атоми се међусобно удружују, градећи стабилне целине. У стабилне целине се удружују најмање два атома истог или различитог хемијског елемента.Грађење стабилних целина описује се грађењем хемијске везе. У зависности од врсте атома који се повезују хемијска веза може бити:
Ковалентна – настаје удруживањем истих или различитих атома неметала.
Јонска – настаје удруживањем атома изразитих метала и атома изразитих неметала.
Све у природи тежи што већој стабилности. Већина атома у природи није стабилна, сем атома племенитих гасова. Због тога се само племенити гасови у природи могу наћи у облику слободних атома. Атоми осталих хемијских елемената се удружују да би створили стабилне целине.
Атоми племенитих гасова се у природи могу наћи у слободном стању јер они у последњем енергетском нивоу поседују по осам електрона, изузев хелијума који има попуњен само један енергетски ниво у коме се налазе два електрона, што је и максималан број електрона за први енергетски ниво. Тако да кажемо да племенити гасови поседују стабилан октет односно стабилан дублет електрона.
Овом броју електрона у последњем енергетском нивоу теже сви остали атоми у природи. Због ове тежње атоми се међусобно удружују, градећи стабилне целине. У стабилне целине се удружују најмање два атома истог или различитог хемијског елемента.Грађење стабилних целина описује се грађењем хемијске везе. У зависности од врсте атома који се повезују хемијска веза може бити:
Ковалентна – настаје удруживањем истих или различитих атома неметала.
Јонска – настаје удруживањем атома изразитих метала и атома изразитих неметала.
Молекули. Хемијске формуле
Повезивањем атома настају нове честице које се понашају другачије од слободних атома. Удружени атоми више нису независни једни од других.
Стабилне целине удружених атома се називају молекули. Постоје молекули елемената и молекули једињења. Молекули елемената настају удруживањем атома истог неметала, молекули једињења настају удруживањем атома различитих неметала.
Удружене атоме представљамо хемијским формулама, слично као што се атоми представљају хемијским симболима.
Постоје три врсте хемијских фомула:
– Н - Н структурне формуле – њих приказујемо тако што електроне који учествују у формирању хемијске везе приказујемо цртицом
– Н : Н електронске формуле – то су формуле у којима електроне који учествују у формирању хемијске везе приказујемо као тачкице
– Н2 молекулске формуле
Тачан број атома неког хемијског елемента означава се индексом. Индекси се пишу у доњем десном углу иза симбола хемијског елемента. Индекс један се никада не пише.
Свака хемијска формула има два значења:
• квалитативно значење – показује врсту атома који изграђују стабилну целину
• квантитативно занчење – показује тачан број атома појединих елемената у стабилној целини и бројчани однос појединачних атома у стабилној целини.
Ако желимо да прикажемо више молекула неког елемента то можемо тако што испред хемијске формуле ставимо број. Тај број се назива коефицијент. Коефицијент један се никад не пише.
Повезивањем атома настају нове честице које се понашају другачије од слободних атома. Удружени атоми више нису независни једни од других.
Стабилне целине удружених атома се називају молекули. Постоје молекули елемената и молекули једињења. Молекули елемената настају удруживањем атома истог неметала, молекули једињења настају удруживањем атома различитих неметала.
Удружене атоме представљамо хемијским формулама, слично као што се атоми представљају хемијским симболима.
Постоје три врсте хемијских фомула:
– Н - Н структурне формуле – њих приказујемо тако што електроне који учествују у формирању хемијске везе приказујемо цртицом
– Н : Н електронске формуле – то су формуле у којима електроне који учествују у формирању хемијске везе приказујемо као тачкице
– Н2 молекулске формуле
Тачан број атома неког хемијског елемента означава се индексом. Индекси се пишу у доњем десном углу иза симбола хемијског елемента. Индекс један се никада не пише.
Свака хемијска формула има два значења:
• квалитативно значење – показује врсту атома који изграђују стабилну целину
• квантитативно занчење – показује тачан број атома појединих елемената у стабилној целини и бројчани однос појединачних атома у стабилној целини.
Ако желимо да прикажемо више молекула неког елемента то можемо тако што испред хемијске формуле ставимо број. Тај број се назива коефицијент. Коефицијент један се никад не пише.
Ковалентна веза
Неметали су у таблици Периодног система елемената смештени у горњем десном углу. Атоми неметала у валентном нивоу имају велики број електрона и недостаје им неколико електрона да би постигли стабилан дублет или октет најближег племенитог гаса, тј. стабилну електронску структуру најближег племенитог гаса.
Атом водоника тежи да постигне стабилну електронску структуру најближег племенитог гаса – хелијума. Хелијум има дублет валентних електрона. Дакле, водоник тежи да постигне стабилан дублет електрона. Овакву структуру може постићи удруживањем једног свог електрона са још једним атомом водоника који такође има један електрон који је уједно и валентни.
Када се два атома водоника приближе један другом, простор у коме се крећу њихови електрони се делимично преклопи. То преклапање омогућава да електрони и једног и другог атома буду под утицајем оба језгра. Електрони почињу да се крећу и око једног и око другог језгра и због тога се називају заједнички електрони. Оба електрона подједнако припадају и једном и другом атому па се овај пар електрона назива заједнички електронски пар.
Веза која настаје образовањем заједничког електронског пара назива се ковалентна веза.
Н . + . Н → Н : Н
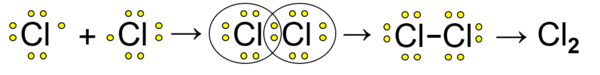
Хлор у последњем енергетском нивоу има седам електрона. До стабилног октета недостаје му један електрон. Атоми хлора теже да постигну стабилну електронску структуру аргона. То ће постићи ако удружи један свој електрон са једним електроном другог атома хлора. На тај начин настаје заједнички електронски пар, који је равномерно распоређен између језгра оба атома и подједнако припада и једном и другом атому. Оваква веза назива се неполарна ковалентна веза. Пошто настаје образовањем једног заједничког електронског пара ова веза је и једнострука.
Атом кисеоника има шест валентних електрона. Недостају му два електрона да би постигао стабилан октет. Ако атом кисеоника удружи своја два електрона са два електрона другог атома кисеоника, оба ће постићи стабилан октет. При томе настају два заједничка електронска пара. Оваква веза се назива двострука ковалентна веза.
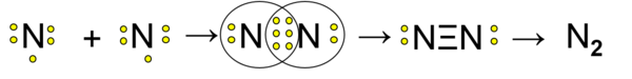
Атом азота има пет валентних електрона. Недостају му три електрона до стабилног октета. Ако атом азота удружи својa три електрона са другим атомом азота, оба атома ће постићи стабилан октет. При томе настају три заједничка електронска пара. Оваква веза назива се трострука ковалентна веза.
Молекули једињења настају када се ковалентним везама повезују нпр. атом водоника и атом хлора:
.. ..
H ∙ + ∙ Cl : → H : Cl :
.. ..
У молекулу хлороводоника сила којом атом хлора привлачи заједнички електронски пар јача је од силе којом атом водоника привлачи тај пар. Тако се на једној страни молекула хлороводоника налази вишак негативног наелектрисања, а на другој страни вишак позитивног наелектрисања. То значи да у молекулу хлороводоника постоје два пола и такав молекул назива се дипол.
.. ..
H ∙ + ∙ Cl : → H : Cl :
.. ..
У молекулу хлороводоника сила којом атом хлора привлачи заједнички електронски пар јача је од силе којом атом водоника привлачи тај пар. Тако се на једној страни молекула хлороводоника налази вишак негативног наелектрисања, а на другој страни вишак позитивног наелектрисања. То значи да у молекулу хлороводоника постоје два пола и такав молекул назива се дипол.
Оваква веза се назива поларна ковалентна веза.
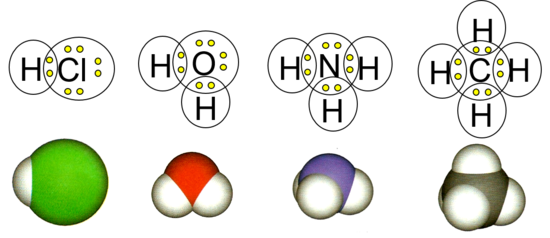
Неметали могу да граде и вишеатомне молекуле. У молекулу воде граде се две једноструке везе између атома кисеоника и два атома водоника. На овај начин кисеоник постиже стабилан октет, а водоник стабилан дублет.
.. ..
H ∙ + ∙ O ∙ + ∙ H → H : O : H
.. ..
Обе ковалентне везе су поларне, јер атом кисеоника јаче привлачи себи електроне заједничких електронских парова него атоми водоника. Део молекула воде где је кисеоник је негативан пол, а део где се налазе атоми водоника је позитиван пол. Молекули воде су диполи.
Неметали могу да граде и вишеатомне молекуле. У молекулу воде граде се две једноструке везе између атома кисеоника и два атома водоника. На овај начин кисеоник постиже стабилан октет, а водоник стабилан дублет.
.. ..
H ∙ + ∙ O ∙ + ∙ H → H : O : H
.. ..
Обе ковалентне везе су поларне, јер атом кисеоника јаче привлачи себи електроне заједничких електронских парова него атоми водоника. Део молекула воде где је кисеоник је негативан пол, а део где се налазе атоми водоника је позитиван пол. Молекули воде су диполи.
Питања и одговори:
1. Да ли у природи постоје слободни атоми?
- Да.
2. Који су то атоми?
- То су атоми племенитих гасова.
3. Зашто само атоми племенитих гасова могу бити у слободном стању у природи?
- Атоми племенитих гасова у последњем енергетском нивоу поседују максималан број електрона, тј. поседују октет или дублет електрона.
4. Чему теже сви остали атоми у природи?
- Сви остали атоми у природи теже да постигну стабилан октет или дублет.
5. Како то могу постићи?
- Могу постићи образовањем хемијске везе
6. Шта је хемијска веза?
- Хемијска везе је сила која држи атоме удружене у стабилну целину.
7. Које врсте хемијске везе постоје?
- Постоје ковалентна и јонска веза.
8. Између којих атома се формира ковалентна веза?
- Ковалентна веза се формира између истих или различитих атома неметала.
9. Шта је ковалентна веза?
– Ковалентна веза настаје образовањем једног или више заједничких електронских парова.
10. Шта су молекули?
– Молекули су стабилне целине удружених атома.
11. Какви могу бити молекули?
– Молекули елемената и молекули једињења.
12. Како настају молекули елемената?
– Настају удруживањем атома истог хемијског елемента.
13. Како настају молекули једињења?
– Настају удруживањем атома различитих хемијских елемената.
14. Колико заједничких електронских парова може настати између два атома?
- Један, два или три.
15. Какве ковалентне везе постоје?
- Ако се формира један електронски пар то је једнострука ковалентна веза, два двострука и три трострука ковалентна веза.
16. Како се још дели ковалентна веза?
- Постоји неполарна (између истих атома) и поларна (између различитих атома).
1. Да ли у природи постоје слободни атоми?
- Да.
2. Који су то атоми?
- То су атоми племенитих гасова.
3. Зашто само атоми племенитих гасова могу бити у слободном стању у природи?
- Атоми племенитих гасова у последњем енергетском нивоу поседују максималан број електрона, тј. поседују октет или дублет електрона.
4. Чему теже сви остали атоми у природи?
- Сви остали атоми у природи теже да постигну стабилан октет или дублет.
5. Како то могу постићи?
- Могу постићи образовањем хемијске везе
6. Шта је хемијска веза?
- Хемијска везе је сила која држи атоме удружене у стабилну целину.
7. Које врсте хемијске везе постоје?
- Постоје ковалентна и јонска веза.
8. Између којих атома се формира ковалентна веза?
- Ковалентна веза се формира између истих или различитих атома неметала.
9. Шта је ковалентна веза?
– Ковалентна веза настаје образовањем једног или више заједничких електронских парова.
10. Шта су молекули?
– Молекули су стабилне целине удружених атома.
11. Какви могу бити молекули?
– Молекули елемената и молекули једињења.
12. Како настају молекули елемената?
– Настају удруживањем атома истог хемијског елемента.
13. Како настају молекули једињења?
– Настају удруживањем атома различитих хемијских елемената.
14. Колико заједничких електронских парова може настати између два атома?
- Један, два или три.
15. Какве ковалентне везе постоје?
- Ако се формира један електронски пар то је једнострука ковалентна веза, два двострука и три трострука ковалентна веза.
16. Како се још дели ковалентна веза?
- Постоји неполарна (између истих атома) и поларна (између различитих атома).