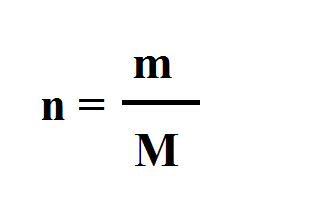- Почетна
-
Седми разред
-
Осми разред
- Неметали, оксиди неметала, киселине >
- Метали, оксиди метала и хидроксиди (базе) >
- Соли >
- Електролитичка дисоцијација киселина, хи >
- Неметали, метали и соли (утврђивање)
- Увод у органску хемију >
- Угљоводоници >
- Органска једињења са кисеоником >
- Биолошки важна органска једињења >
- Хемија животне средине >
- Провери своје знање (средња школа)
- Периодни систем елемената
- Занимљивости из света хемије
- Моја хемија
Како се рачуна количина неке супстанце?
n = m / M
m - маса супстанце (g)
М - моларна маса (g/mol)
Јединица mol.
n = m / M
m - маса супстанце (g)
М - моларна маса (g/mol)
Јединица mol.
1. Ако се одмери 90 грама воде, колико је то молова воде?
Mr (H2O)= 2· Ar (H) + Ar (O) = 2 · 1 + 16 = 18
M = Mr · g/mol
M = 18 g/mol
m = 90 g
n = ?
n = m / M
n = 90 g / 18 g/mol
n = 5 mol
2. Коликa je маса 2 mol-а амонијака, NH3?
Mr (NH3)= Ar (N) + 3 · Ar (H) = 14 + 3 · 1 = 17
M = Mr · g/mol
M = 17 g/mol
m = ?
n = 2 mol
n = m / M
m = n · M
m = 2 mol · 17 g/mol = 34 g
Како се рачуна број честица неке супстанце?
n = N / Na
N - број честица (атома, молекула или јона)
Nа - Авогадров број
3. Колико молекула има у 3 mol-a метана, CH4?
N = ?
n = 3 mol
Nа = 6 · 10²³ molekula/mol
n = N / Na
N = n · Na
N = 3 mol · 6 · 10²³ molekula/mol
N = 18 · 10²³ molekula
Задаци:
1. Колика је маса 2 мола натријум - хидроксида, NaOH?
2. Колико има атома у 3 мола неона, Ne?
3. Колико је молова 6,4 грама сумпор - диоксида, SO2?
Mr (H2O)= 2· Ar (H) + Ar (O) = 2 · 1 + 16 = 18
M = Mr · g/mol
M = 18 g/mol
m = 90 g
n = ?
n = m / M
n = 90 g / 18 g/mol
n = 5 mol
2. Коликa je маса 2 mol-а амонијака, NH3?
Mr (NH3)= Ar (N) + 3 · Ar (H) = 14 + 3 · 1 = 17
M = Mr · g/mol
M = 17 g/mol
m = ?
n = 2 mol
n = m / M
m = n · M
m = 2 mol · 17 g/mol = 34 g
Како се рачуна број честица неке супстанце?
n = N / Na
N - број честица (атома, молекула или јона)
Nа - Авогадров број
3. Колико молекула има у 3 mol-a метана, CH4?
N = ?
n = 3 mol
Nа = 6 · 10²³ molekula/mol
n = N / Na
N = n · Na
N = 3 mol · 6 · 10²³ molekula/mol
N = 18 · 10²³ molekula
Задаци:
1. Колика је маса 2 мола натријум - хидроксида, NaOH?
2. Колико има атома у 3 мола неона, Ne?
3. Колико је молова 6,4 грама сумпор - диоксида, SO2?