- Почетна
-
Седми разред
-
Осми разред
- Неметали, оксиди неметала, киселине >
- Метали, оксиди метала и хидроксиди (базе) >
- Соли >
- Електролитичка дисоцијација киселина, хи >
- Неметали, метали и соли (утврђивање)
- Увод у органску хемију >
- Угљоводоници >
- Органска једињења са кисеоником >
- Биолошки важна органска једињења >
- Хемија животне средине >
- Провери своје знање (средња школа)
- Периодни систем елемената
- Занимљивости из света хемије
- Моја хемија
1. Шта су хемијске реакције?
Промене током којих из једне или више супстанци настају нове супстанце називају се хемијске промене, хемијске реакције или хемијски процеси.
2. Како препознајемо да ли је дошло до хемијске промене, односно да ли је дошло до настанка нове супстанце?
Постоје више начина да се одреди да ли је током промене настала нова супстанца (појава талога, мехурића гаса и промене боје).
3. Како се приказују хемијске реакције?
Хемијске реакције приказују се хемијским једначинама.
Реакцијом између соде бикарбоне и сирћетне киселине, ослобађају се мехурићи угљендиоксида.
NaHCO3 + CH3COOH → CH3COONa + CO2↑ + H2O
Реакција сагоревања траке магнезијума (види се бљештава бела светлост и добија се бела прашкаста супстанца магнезијум(II)-оксида).
2Mg + O2 → 2MgO
Реакцијом између натријум-хлорида и сребро-нитрата ствара се бели сирасти талог сребро-хлорида.
NaCl + AgNO3 → AgCl↓ + NaNO3
4. Како састављамо једначине хемијских реакција?
На левој страни једначине (лево од стрелице) одговарајућим ознакама, симболима или хемијским формулама, представљају се реактанти (супстанце које реагују), а на десној (десно од стрелице) реакциони производи (супстанце које настају у реакцији).
реактант 1 + реактант 2 → производ 1 + производ 2
5. Која су два основна типа хемијских реакција?
То су синтеза (сједињавање) и анализа (разлагање).
6. Шта је анализа?
Реакција растављања чисте супстанце на две или више чистих супстанци назива се анализа.
7. Примери реакција анализа?
Разлагањем шећера добија се угљеник и вода.
C12H22O11 → 12C + 11 H2O
једињење елемент једињење
Пропуштањем струје код воду, вода се разлаже на кисеоник и водоник.
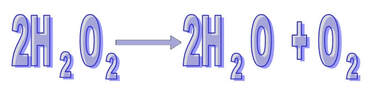
2H2O → 2H2 + O2
једињење елемент елемент
Жарењем кречњака добија се живи (негашени) креч и угљеник(IV)-оксид.
CaCO3 загревање → CaO + CO2
једињење једињење једињење
8. Шта се добија у реакцијама анализе?
Анализом чисте супстанце могу се добити два елемента, елемент и једињење или два једноставнија једињења.
9. Шта је синтеза?
Реакција стварања нове супстанце од две или више чистих супстанци назива се синтеза.
10. Примери реакција синтезе?
Реакцијом сагоревања траке магнезијума добија се бела прашкаста супстанца магнезијум(II)-оксида.
2Mg + O2 → 2MgO
елемент елемент једињење
Реакцијом између угљендиоксида и воде добија се угљена киселина.
CO2 + H2O → H2CO3
једињење једињење једињење
11. Да ли су реакције синтезе и анализе повезане?
Да. Ако напишемо Fe + S → FeS то је реакција синтезе (сједињавања) гвожђе(II)-сулфида из гвожђа и сумпора, ако напишемо FeS → Fe + S то је реакција анализе (разлагања) гвожђе(II)-сулфида на гвожђе и сумпор. Реактанти у реакцији синтезе су производи у реакцији анализе.
Питања:
1. Шта је анализа, а шта синтеза?
2. а) Одреди која реакција је реакција анализе, а која реакција синтезе?
б) Сваку реакцију прикажи у супротном смеру (односно анализу као синтезу, а синтезу као анализу)?