- Почетна
-
Седми разред
-
Осми разред
- Неметали, оксиди неметала, киселине >
- Метали, оксиди метала и хидроксиди (базе) >
- Соли >
- Електролитичка дисоцијација киселина, хи >
- Неметали, метали и соли (утврђивање)
- Увод у органску хемију >
- Угљоводоници >
- Органска једињења са кисеоником >
- Биолошки важна органска једињења >
- Хемија животне средине >
- Провери своје знање (средња школа)
- Периодни систем елемената
- Занимљивости из света хемије
- Моја хемија
1. Шта су киселине? Како се лакмус-папир понаша у киселој средини? Како киселине дисосују у води?
- Киселине су супстанце које се састоје од водоника и киселинског остатка и у воденом раствору дисосују (разлажу се) на позитиван јон водоника и негативан јон киселинског остатка, плави лакмус папир боје у црвени.
2. Шта су базе? Како се лакмус папир понаша у базној средини? Како базе дисосују у води?
- Базе се састоје од метала и хидроксидне групе и у воденом раствору дисосују (разлажу се) на позитиван јон метала и негативан јон хидроксидне групе, црвени лакмус папир боје у плави.
Можемо извести закључак да су киселине и базе супстанце са супротним особинама.
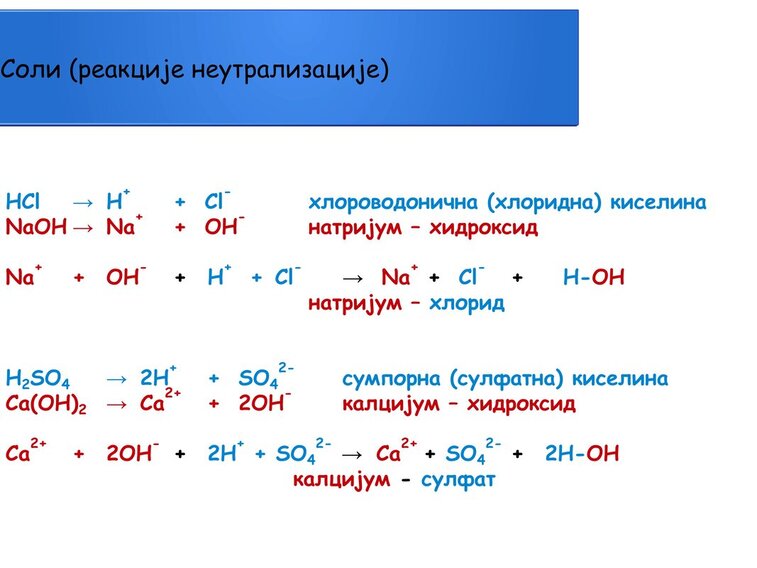
Киселине имају киселе особине, базе базне и када помешамо њихове водене растворе долази до хемијске реакције. Ове реакције зову се реакције неутрализације.
- Киселине су супстанце које се састоје од водоника и киселинског остатка и у воденом раствору дисосују (разлажу се) на позитиван јон водоника и негативан јон киселинског остатка, плави лакмус папир боје у црвени.
2. Шта су базе? Како се лакмус папир понаша у базној средини? Како базе дисосују у води?
- Базе се састоје од метала и хидроксидне групе и у воденом раствору дисосују (разлажу се) на позитиван јон метала и негативан јон хидроксидне групе, црвени лакмус папир боје у плави.
Можемо извести закључак да су киселине и базе супстанце са супротним особинама.
Киселине имају киселе особине, базе базне и када помешамо њихове водене растворе долази до хемијске реакције. Ове реакције зову се реакције неутрализације.
Соли су јонска једињења која се састоје од катјона метала и анјона киселинског остатка. Постоје и соли које у свом саставу немају метал, већ амонијумов јон, који је једновалентан и те соли се називају амонијумове соли.
Име добијају тако што се на име метала или амонијум јона дода име киселинског остатка. Када је потребно (код метала променљиве валенце), иза имена метала наводи се његова валенца (на пример, FeCl3 - гвожђе (III)-хлорид, NaCl - натријум-хлорид, CaSO4 - калцијум-сулфат, Na2CO3 - натријум- карбонат, Ca(NO3)2 - калцијум-нитрат, NH4Cl - амонијум-хлорид, (NH4)2SO4 - амонијум - сулфат).
Соли настају од киселина заменом водоникових атома атомима метала. Водоникови јони се замењују позитивним јонима метала. Киселински остаци остају као анјони и наелектрисани су негативно онолико пута колико је било водоникових атома у киселини.
HCl - хлороводонична (хлоридна) киселина, има један водоников атом, Cl¯- хлоридни јон (наелектрисан -).
HNO3 - азотна (нитратна) киселина, има један водоников атом, NO3¯- нитратни јон (наелектрисан -).
H2SO4 - сумпорна (сулфатна) киселина, има два водоникова атома, SO4²¯- сулфатни јон (наелектрисан 2-).
H2CO3 - угљена (карбонатна) киселина, има два водоникова атома, CO3 ²¯ - карбонатни јон (наелектрисан 2-).
Када се у киселинама које имају више водоникових атома замене сви водоникови атоми добијају се неутралне соли, ако се не замене сви водоникови атоми добијају се киселе соли, на пример натријум, Na, замени само један водоник у угљеној (карбонатној) киселини, H2CO3, настаје натријум - хидрогенкарбонат, NaHCO3 или ако натријум, Na, замени само један водоник у фосфорној киселини (фосфатној) киселини, H3PO4, настаје натријум - дихидрогенфосфат, NaH2PO4. Постоје и базне соли које поред катјона метала имају једну или више хидроксидних група, (MgOH)3PO4 - магнезијум-хидроксидфосфат.
2NaOH + H2CO3 = Na2CO3 + 2H2O натријум-карбонат (неутрална со)
NaOH + H2CO3 = NaHCO3 + H2O натријум-хидрогенкарбонат (кисела со)
3Mg(OH)2 + 2H3PO4 = Mg3(PO4)2 + 6H2O магнезијум-фосфат (неутрална со)
Mg(OH)2 + H3PO4 = MgHPO4 + 2H2O магнезијум-хидрогенфосфат (кисела со)
Mg(OH)2 + 2H3PO4 = Mg(H2PO4)2 + 2H2O магнезијум-дихидрогенфосфат (кисела со)
3Mg(OH)2 + H3PO4 = (MgOH)3PO4 + 3H2O магнезијум-хидроксидфосфат (базна со)
Питања и одговори:
1. Шта су соли?
- Соли су чврста јонска једињења, састоје се од метала и киселинског остатка.
2. Шта је неутрализација?
- То је реакција између киселина и база.
3. Навести неколико киселина, њихова имена и како се зову соли те киселине?
Хлоридна киселина – хлориди, Cl-, сулфатна – сулфати, SO4²¯, нитратна – нитрати, NO3¯ карбонатна – карбонати, CO3 ²¯.
4. Како се деле соли?
- На неутралне, киселе и базне.
Име добијају тако што се на име метала или амонијум јона дода име киселинског остатка. Када је потребно (код метала променљиве валенце), иза имена метала наводи се његова валенца (на пример, FeCl3 - гвожђе (III)-хлорид, NaCl - натријум-хлорид, CaSO4 - калцијум-сулфат, Na2CO3 - натријум- карбонат, Ca(NO3)2 - калцијум-нитрат, NH4Cl - амонијум-хлорид, (NH4)2SO4 - амонијум - сулфат).
Соли настају од киселина заменом водоникових атома атомима метала. Водоникови јони се замењују позитивним јонима метала. Киселински остаци остају као анјони и наелектрисани су негативно онолико пута колико је било водоникових атома у киселини.
HCl - хлороводонична (хлоридна) киселина, има један водоников атом, Cl¯- хлоридни јон (наелектрисан -).
HNO3 - азотна (нитратна) киселина, има један водоников атом, NO3¯- нитратни јон (наелектрисан -).
H2SO4 - сумпорна (сулфатна) киселина, има два водоникова атома, SO4²¯- сулфатни јон (наелектрисан 2-).
H2CO3 - угљена (карбонатна) киселина, има два водоникова атома, CO3 ²¯ - карбонатни јон (наелектрисан 2-).
Када се у киселинама које имају више водоникових атома замене сви водоникови атоми добијају се неутралне соли, ако се не замене сви водоникови атоми добијају се киселе соли, на пример натријум, Na, замени само један водоник у угљеној (карбонатној) киселини, H2CO3, настаје натријум - хидрогенкарбонат, NaHCO3 или ако натријум, Na, замени само један водоник у фосфорној киселини (фосфатној) киселини, H3PO4, настаје натријум - дихидрогенфосфат, NaH2PO4. Постоје и базне соли које поред катјона метала имају једну или више хидроксидних група, (MgOH)3PO4 - магнезијум-хидроксидфосфат.
2NaOH + H2CO3 = Na2CO3 + 2H2O натријум-карбонат (неутрална со)
NaOH + H2CO3 = NaHCO3 + H2O натријум-хидрогенкарбонат (кисела со)
3Mg(OH)2 + 2H3PO4 = Mg3(PO4)2 + 6H2O магнезијум-фосфат (неутрална со)
Mg(OH)2 + H3PO4 = MgHPO4 + 2H2O магнезијум-хидрогенфосфат (кисела со)
Mg(OH)2 + 2H3PO4 = Mg(H2PO4)2 + 2H2O магнезијум-дихидрогенфосфат (кисела со)
3Mg(OH)2 + H3PO4 = (MgOH)3PO4 + 3H2O магнезијум-хидроксидфосфат (базна со)
Питања и одговори:
1. Шта су соли?
- Соли су чврста јонска једињења, састоје се од метала и киселинског остатка.
2. Шта је неутрализација?
- То је реакција између киселина и база.
3. Навести неколико киселина, њихова имена и како се зову соли те киселине?
Хлоридна киселина – хлориди, Cl-, сулфатна – сулфати, SO4²¯, нитратна – нитрати, NO3¯ карбонатна – карбонати, CO3 ²¯.
4. Како се деле соли?
- На неутралне, киселе и базне.