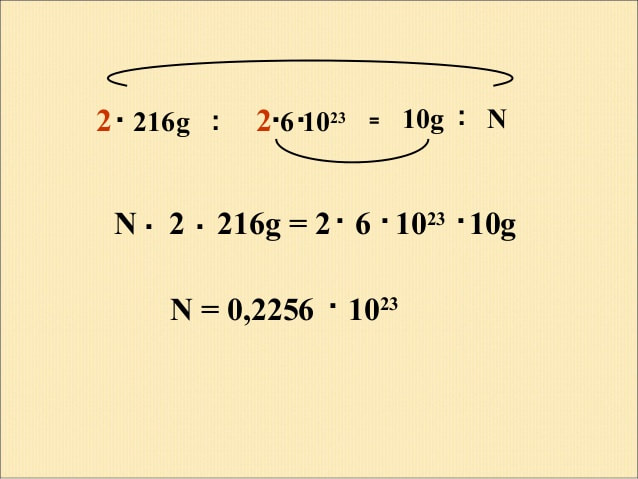- Почетна
-
Седми разред
-
Осми разред
- Неметали, оксиди неметала, киселине >
- Метали, оксиди метала и хидроксиди (базе) >
- Соли >
- Електролитичка дисоцијација киселина, хи >
- Неметали, метали и соли (утврђивање)
- Увод у органску хемију >
- Угљоводоници >
- Органска једињења са кисеоником >
- Биолошки важна органска једињења >
- Хемија животне средине >
- Провери своје знање (средња школа)
- Периодни систем елемената
- Занимљивости из света хемије
- Моја хемија
Стехиометрија је област хемије која се бави израчунавањима на основу једначине хемијске реакције.
За израчунавање на основу хемијске једначине, најпре, је потребно исправно саставити једначину хемијске реакције.
Свака једначина хемијске реакције има квалитативно и квантитативно значење. На пример:
3H2 + N2 = 2NH3
Из једначине видимо да три молекула водоника реагују са једним молекулом азота и при томе настају два молекула амонијака.
У кантитативном значењу ова једначина се тумачи на следећи начин: три мола водоника реагују са једним молом азота и настају два мола амонијака. Пошто мол садржи увек исти број честица, однос броја молекула водоника, азота и амонијака, остаје 3:2:1.
3H2 + N2 = 2NH3
n
3 mol водоника
1 mol азота
2 mol амонијака
m
(m = n · M)
3 mol · 2 g/mol = 6g водоника
1 mol · 28 g/mol = 28g азота
2 mol · 17 g/mol = 34g амонијака
N
(N = n · NA)
3 · 6 · 10²³ молекула водоника
1 · 6 · 10²³ молекула азота
2 · 6 · 10²³ молекула амонијака
1. Колико се молова амонијака добија у реакцији 4 мола водоника са азотом?
Из једначине видимо да 3 мола водоника даје 2 мола амонијака, постављамо пропорцију
3 mol (H2) : 2 mol (NH3) = 4 mol (H2) : X mol (NH3)
3 mol · X mol = 2 mol · 4 mol
X = 2 mol · 4 mol / 3 mol
X = 2,66 mol NH3
2. Колико грама амонијака се добија у реакцији 6 молова водоника са азотом?
Из реакције видимо да 3 мола водоника даје 34g амонијака, постављамо пропорцију
3 mol (H2) : 34 g (NH3) = 6 mol (H2) : X g (NH3)
3 mol · X g = 34 g · 6 mol
X = 34 g · 6 mol / 3 mol
X = 68 g
3. Колико молова магнезијум-оксида настаје у реакцији оксидације 6g магнезијума?
Прво напишемо и изједначимо једначину ове хемијске реакције:
2Mg + O2 = 2MgO
Из једначине видимо да 2 мола магнезијума реагује са једним молом кисеоника и настаје 2 мола магнезијум-оксида, односно 48 g магнезијума реагује са 32 g кисеоника и настаје 80 g магнезијум-оксида
(Ar (Mg) = 24 и његова маса m = 2 mol · 24 g/mol = 48 g,
Ar(O) = 16, Mr (O2) = 2 · Ar(O) = 2 · 16 = 32 и маса кисеоника је m = 1 mol · 32 g/mol = 32 g,
Mr (MgO) = 24 + 16 = 40 и маса магнезијум-оксида је m = 2 mol · 40 g/mol = 80 g)
6g X mol
2Mg + O2 = 2MgO
2 mol 1 mol 2 mol
48g 32g 80g
Онда поставимо пропорцију: ако из 48g магнезијума настаје 2 мола магнезијум-оксида колико настаје из 6g.
48g (Mg) : 2 mol (MgO) = 6g : X mol
48g · X mol = 6g · 2 mol
X = 6g · 2 mol / 48g = 0,25 mol
4. Колико молекула магнезијум-оксида настаје када магнезијум реагује са 6 молова кисеоника?
6 mol X молекула
2Mg + O2 = 2MgO
2 mol 1 mol 2 mol
2 · 6 · 10²³ молекула Mg, 6 · 10²³ молекула O2, 2 · 6 · 10²³ молекула MgO
Онда поставимо пропорцију: ако из 1 мола кисеоника настаје 2 · 6 · 10²³ молекула магнезијум-оксида колико настаје из 6 молова.
1 mol (O2 ) : 2 · 6 · 10²³ молекула (MgO) = 6 mol : X молекула
X = 6 mol · 2 · 6 · 10²³ молекула/mol
X = 72 · 10²³ молекула
5. Колико атома живе настаје реакцијом разлагања 10 грама жива (II)-оксида?
За израчунавање на основу хемијске једначине, најпре, је потребно исправно саставити једначину хемијске реакције.
Свака једначина хемијске реакције има квалитативно и квантитативно значење. На пример:
3H2 + N2 = 2NH3
Из једначине видимо да три молекула водоника реагују са једним молекулом азота и при томе настају два молекула амонијака.
У кантитативном значењу ова једначина се тумачи на следећи начин: три мола водоника реагују са једним молом азота и настају два мола амонијака. Пошто мол садржи увек исти број честица, однос броја молекула водоника, азота и амонијака, остаје 3:2:1.
3H2 + N2 = 2NH3
n
3 mol водоника
1 mol азота
2 mol амонијака
m
(m = n · M)
3 mol · 2 g/mol = 6g водоника
1 mol · 28 g/mol = 28g азота
2 mol · 17 g/mol = 34g амонијака
N
(N = n · NA)
3 · 6 · 10²³ молекула водоника
1 · 6 · 10²³ молекула азота
2 · 6 · 10²³ молекула амонијака
1. Колико се молова амонијака добија у реакцији 4 мола водоника са азотом?
Из једначине видимо да 3 мола водоника даје 2 мола амонијака, постављамо пропорцију
3 mol (H2) : 2 mol (NH3) = 4 mol (H2) : X mol (NH3)
3 mol · X mol = 2 mol · 4 mol
X = 2 mol · 4 mol / 3 mol
X = 2,66 mol NH3
2. Колико грама амонијака се добија у реакцији 6 молова водоника са азотом?
Из реакције видимо да 3 мола водоника даје 34g амонијака, постављамо пропорцију
3 mol (H2) : 34 g (NH3) = 6 mol (H2) : X g (NH3)
3 mol · X g = 34 g · 6 mol
X = 34 g · 6 mol / 3 mol
X = 68 g
3. Колико молова магнезијум-оксида настаје у реакцији оксидације 6g магнезијума?
Прво напишемо и изједначимо једначину ове хемијске реакције:
2Mg + O2 = 2MgO
Из једначине видимо да 2 мола магнезијума реагује са једним молом кисеоника и настаје 2 мола магнезијум-оксида, односно 48 g магнезијума реагује са 32 g кисеоника и настаје 80 g магнезијум-оксида
(Ar (Mg) = 24 и његова маса m = 2 mol · 24 g/mol = 48 g,
Ar(O) = 16, Mr (O2) = 2 · Ar(O) = 2 · 16 = 32 и маса кисеоника је m = 1 mol · 32 g/mol = 32 g,
Mr (MgO) = 24 + 16 = 40 и маса магнезијум-оксида је m = 2 mol · 40 g/mol = 80 g)
6g X mol
2Mg + O2 = 2MgO
2 mol 1 mol 2 mol
48g 32g 80g
Онда поставимо пропорцију: ако из 48g магнезијума настаје 2 мола магнезијум-оксида колико настаје из 6g.
48g (Mg) : 2 mol (MgO) = 6g : X mol
48g · X mol = 6g · 2 mol
X = 6g · 2 mol / 48g = 0,25 mol
4. Колико молекула магнезијум-оксида настаје када магнезијум реагује са 6 молова кисеоника?
6 mol X молекула
2Mg + O2 = 2MgO
2 mol 1 mol 2 mol
2 · 6 · 10²³ молекула Mg, 6 · 10²³ молекула O2, 2 · 6 · 10²³ молекула MgO
Онда поставимо пропорцију: ако из 1 мола кисеоника настаје 2 · 6 · 10²³ молекула магнезијум-оксида колико настаје из 6 молова.
1 mol (O2 ) : 2 · 6 · 10²³ молекула (MgO) = 6 mol : X молекула
X = 6 mol · 2 · 6 · 10²³ молекула/mol
X = 72 · 10²³ молекула
5. Колико атома живе настаје реакцијом разлагања 10 грама жива (II)-оксида?
Задаци за вежбање:
1. Колико грама гвожђе(II)-сулфида настаје ако реагује 16 грама сумпора и довољна количина гвожђа?
2. Колико молова калцијума је реаговало ако је у реакцији са кисеоником настало 0,5 мола калцијум-оксида?
3. Колико грама воде се добија ако 5 молова водоника реагује са кисеоником?
4. Колико молова кухињске соли настаје ако 46 грама натријума реагује са хлором?
5. Колико молекула амонијака настаје када 6 молова азота реагује са водоником?
1. Колико грама гвожђе(II)-сулфида настаје ако реагује 16 грама сумпора и довољна количина гвожђа?
2. Колико молова калцијума је реаговало ако је у реакцији са кисеоником настало 0,5 мола калцијум-оксида?
3. Колико грама воде се добија ако 5 молова водоника реагује са кисеоником?
4. Колико молова кухињске соли настаје ако 46 грама натријума реагује са хлором?
5. Колико молекула амонијака настаје када 6 молова азота реагује са водоником?